Аннотация
Цель: В современной клинической терапевтической практике широкое применение нашли средства
электрофизического воздействия, работающие в радиочастотном диапазоне, благодаря оказываемым ими
тепловым
эффектам, направленным, главным образом, на облегчение боли и воспаления, а также на улучшение
растяжимости
тканей. Наиболее распространенными и лучше всего изученными среди них являются средства
терапевтического
воздействия, работающие в коротковолновом диапазоне на частоте 27,12 МГц. Кроме того, несмотря на
относительную
новизну уже появились и применяются средства электрофизического терапевтического воздействия,
работающие в
гораздо более низком диапазоне частот. Одной из таких новаторских процедур является терапия,
основанная на
действии электротоков емкостно-резистивной монополярной радиочастоты равной 448 кГц. Проведенное
лабораторное
исследование было направлено на изучение тепловых ответов кожи на радиочастотную терапию 448 кГц у
здоровых
взрослых пациентов. Методы: Рандомизированное перекрестное исследование 2х групп предусматривало
участие 15
добровольцев в радиочастотной терапии с частотой 448 кГц, состоящей из двух режимов (емкостного и
резистивного),
с применением аппарата Indiba, которая проводилась локально на участке в нижней части бедра.
Интенсивность
воздействия с минимального постепенно увеличивалась до ощущения теплового дискомфорта. Участников
просили
сообщать о трех контрольных моментах: начало теплового ощущения, четко выраженное тепловое ощущение
и начало
теплового дискомфорта. Температуру кожи измеряли локально до, сразу после и через 45 минут после
терапии.
Полученные результаты: Значительное повышение температуры кожи наблюдалось как емкостном,
так и
резистивном режиме терапии, и температура удерживалась на этом уровне в течение последующих 45
минут.
Наблюдалась статистически значимая разница между характерами теплового ответа, создаваемыми в двух
режимах
воздействия. Пиковые температуры, достигаемые в период после терапии, не имели существенных различий
в двух
режимах, однако степень удержания температуры в период посттерапевтического наблюдения в резистивном
режиме была
значительно выше. Выводы: Настоящее исследование подтверждает, что радиочастотная терапия с частотой
448 кГц
может вызывать значительное повышение и продолжительное удерживание повышенной температуры кожи.
Исследование
также способствует получению полезных исходных данных для дальнейших исследований низкочастотных
диапазонов
радиочастотной терапии, которые остаются в значительной степени неизученными.
Ключевые слова
Средства электрофизического воздействия, здоровые взрослые, радиочастота, термальная доза, термические эффекты
История
Получена редакцией 15 мая 2015 г.
Пересмотрено 12 августа 2015 г.
Принято к опубликованию 6 сентября 2015 г.
Опубликовано в сети 29 октября 2015 г.
Введение
Средства электрофизического воздействия (EPA) используются терапевтами для лечения самых разных состояний. Некоторые из них могут вызывать гипертермию в тканях неинвазивно и без абляций. Если некоторые средства вызывают поверхностный нагрев участка тела, проходящего терапевтическую процедуру (например, при воздействии инфракрасными (ИК) лучами), другие, такие как электрофизические средства, основанные на действии электромагнитного поля радиочастот (ЭМП РЧ или просто РЧ), способны нагревать как кожу, так и более глубокие структуры (например, мышцы и ткани суставов) [1].
Физиологическое воздействие тепла на живые ткани подтверждается большим количеством соответствующих исследований. Тепло способно вызвать изменения в поверхностных и глубоких тканях на клеточном и системном уровнях. Даже умеренного повышения температуры (легкой гипертермии) достаточно для ускорения и (или) увеличения активности большинства клеток, а тепловая вазодилатация способна улучшить кровообращение на участках тканей [1-3]. Тепло также может изменить характер соединительных тканей. Оно может повлиять на изменение свойств сухожилий, связок и, в некоторой степени, мышц за счет увеличения растяжимости, а также уменьшения их тонуса и спазма [1-3]. Степень вызываемого физиологического эффекта может быть разной в зависимости от уровня воздействия.
В терапии тепловое воздействие зачастую используется как способ облегчить боль и воспаление, а также потенциально улучшить заживление тканей. Считается, что в основе теплового воздействия на боль и восстановление тканей лежат различные физиологические механизмы, в том числе, помимо прочего, изменения, возникающие в результате увеличения кровотока, поглощения кислорода и скорости химических реакций. С терапевтической точки зрения повышение температуры ткани более чем на 1°С помогает снять легкое воспаление, повышение на 2-3°С способно уменьшить боль и мышечный спазм, а повышение на 3-4°С может вызвать изменения в растяжимости ткани [3,4]. Повышение температуры в подобном диапазоне, используемое в клинической терапевтической практике, это лишь «легкая гипертермия», в то время как многие другие инвазивные и цитотоксические медицинские процедуры (например, радиочастотная абляция) вызывают значительно более высокое повышение.
Средства электрофизического воздействия в радиочастотном диапазоне применяются в терапевтической практике для теплового воздействия различной степени с первых десятилетий прошлого века [5]. Электромагнитная энергия, передаваемая подобными устройствами, вызывает нагрев тканей в результате колебания и трения заряженных молекул (таких как белки и ионы). Величина повышения температуры сама по себе зависит от электрических свойств тканей и скорости поглощения энергии (удельный коэффициент поглощения – SAR) [1,6].
Одна из технологий электрофизического воздействия, направленная на вызов легкой гипертермии, известная как длинноволновая диатермия (которая использовала радиочастотные поля в диапазоне 0,5–1 МГц) устарела еще в 1950-х годах из-за ограничений практического характера и серьезных помех, которые она вызывала в средствах связи и вещания [7]. Большее распространение в современной терапевтической практике получила коротковолновая терапия (SWT) (известная также как коротковолновая диатермия или SWD), в которой обычно используются токи с частотой 27,12 МГц, и микроволновая терапия (также известная как микроволновая диатермия или MWD), в которой используются токи с частотой до 2,45 ГГц. Однако сейчас во многих странах микроволновая терапия используется все реже [8,9].
При коротковолновой терапии существует 2 режима воздействия: непрерывный (CSWT) и импульсный (PSWT). Непрерывный (CSWT) широко использовался врачами-клиницистами начиная с 1930-х годов, однако последнее время стал менее популярным в западных странах и применяется намного реже [8,10]. Как и во время микроволновой терапии, в непрерывном режиме КВ-терапии (CSWT) обычно вызывается относительно более высокий нагрев тканей по сравнению с импульсным режимом (PSWT), поскольку более низкий нагрев не обеспечивает необходимого «термического вымывания» участков кожи во время сеансов терапии [1]. Снижение популярности КВ-терапии в непрерывном режиме воздействия (CSWT) частично связано с «веяниями моды», а не с одной только публикацией данных, учитывая наличие подтвержденных научно-экспериментальных доказательства в пользу применения CSWT [11].
Разработанный в 40-х годах прошлого века импульсный метод PSWT напротив с тех пор стал более популярным и до сих пор широко используется [8,10,12]. Большинство исследований биологического воздействия радиочастот направлено на изучение более высокого диапазона (микроволн), в особенности в таких областях, как мобильная телефония [13]. При этом, недавний обзор научной литературы, предпринятый авторами настоящего исследования, [14] показал, что РЧ, используемые в настоящее время в клинической терапевтической практике, находятся преимущественно в относительно более низком частотном диапазоне – 30 кГц-30 МГц и даже в большинстве случаев не выходят за рамки 10-30 МГц (в частности PSWT с частотой 27,12 МГц в качестве режима передачи) [8,10,11].
Несмотря на слабую изученность, средства электрофизического воздействия, работающие в значительно более низких радиочастотных диапазонах (< 1 МГц), также были замечены и использовались в клинической практике для вызова легкой гипертермии и другого физиологического воздействия [15-18]. Примером таких средств, используемых в настоящее время в терапевтической практике, является устройство для воздействия током емкостно-резистивной монополярной радиочастоты (CRMRF) равной 448 кГц. Целью настоящего исследования является изучение теплового ответа кожных покровов (тепловых эффектов) на чрескожное воздействие тока емкостно-резистивной монополярной радиочастоты в непрерывном режиме у здоровых взрослых пациентов.
Материалы и методы
Оборудование
Энергетическое воздействие током емкостно-резистивной монополярной радиочастоты выполнялось с применением устройства аппарата Indiba (производства Indiba SA, Барселона, Испания). Оборудование было откалибровано по месту изготовления и предварительно протестировано на погрешность выходной мощности. Пиковая мощность устройства составила 200 Вт (или 450 ВА (Вольт-Ампер)). Подача энергии в РЧ-диапазоне осуществляется в двух режимах: емкостном (ЕМК) и резистивном (РЕЗ). Интенсивность воздействия указана в процентах выходной мощности.
В качестве активных электродов использовали жесткие круглые металлические электроды диаметром 65 мм, а в качестве неактивного электрода использовали крупную гибкую прямоугольную металлическую пластину размером 200 х 260 мм. В качестве контактной среды между электродом и поверхностью кожи использовали проводящий крем, поставляемый производителем. На электрод емкостного воздействия (ЕМК) нанесено полиамидное покрытие, которое действует как диэлектрическая среда, изолируя металлический корпус электрода от поверхности кожи и образуя вместе с испытывающими воздействие тканями электрический конденсатор. На резистивном (РЕЗ) электроде покрытия нет, и он пропускает электроэнергию в РЧ-диапазоне непосредственно через тело на нейтральную пластину. Интенсивность РЧ-воздействия и выходная энергия (Рисунок 1) отображаются на дисплее аппарата, а соответствующие показания по беспроводной связи записываются с помощью компьютерной программы мониторинга в исследовательской среде. Мониторинговое ПО также дает возможность экспорта подробного журнала экспериментальных данных.
Для измерения температуры поверхности кожи и внутренней температуры тела применялись соответственно ручной бесконтактный ИК-термометр для поверхности кожи производства Tecnimed Srl, Ведано-Олона, Италия (Thermofocus 01500A3) и ушной ИК-термометр производства Braun GmbH, Кронберг, Германия (Braun ThermoScan IRT 4520). Поверхностный термометр обладает точностью измерения ± 0,3°C в диапазоне 20,0–42,5°C с повышенной точностью ± 0,2°C в диапазоне 36,0–39,0°C. Ушной термометр имеет точность измерения ± 0,2°C в диапазоне 35,5–42,0°C и ± 0,3°C за пределами диапазона.
Процедура выборки и распределение по группам
Для измерения массы тела, процентного содержания жира в организме, висцерального жира и индекса массы тела (ИМТ) участников применялся анализатор состава тела производства Omron Healthcare Europe B.V., Хофддорп, Нидерланды (Omron BF508). Для подачи звуковых сигналов длительностью 1 и 30 секунд с целью облегчения экспериментального процесса использовались соответственно электронный метроном (производства Seiko Instruments Inc., Токио, Япония) и компьютерный таймер. Контроль комнатной температуры и влажности осуществлялся с помощью электронного термогигрометра производства RS Components Pte Ltd., Сингапур (RS 212124).
В исследовании приняла участие когорта из 15 взрослых без симптомов (со слов самих участников), случайным образом отобранных из 27 000 сотрудников и студентов Университета Хартфордшира. Набор осуществлялся посредством электронных писем, рассылаемых по всему университету. Респондентов последовательно проверяли по критериям пригодности, и таким образом были набраны первые 15 подходящих участником (критерии пригодности более подробно представлены ниже). Все участники подписали осознанное согласие еще до начала исследования. Исследование было одобрено комитетом по этике в области здравоохранения и гуманитарных наук с делегированными полномочиями (HHSECDA) Университета Хартфордшира (номер протокола: HSK/PG/UH/00015). Каждый участник прошел два сеанса терапии – по одному в каждом из режимов ЕМК и РЕЗ, таким образом получились две отдельные группы терапии. Порядок посещения был рандомизирован путем сокрытия с применением электронно-генерируемой схемы рандомизации (IBM SPSS Statistics, версия 20) и скрыт от участников. Контрольных групп или групп плацебо не предусматривалось. Исходя из данных пилотных экспериментов между двумя сеансами предусматривался минимальный перерыв в 48 часов, чтобы избежать проявления остаточного воздействия первого сеанса во время второго. Каждый сеанс у каждого участника проходил в одно и то же время суток (± 1 час).
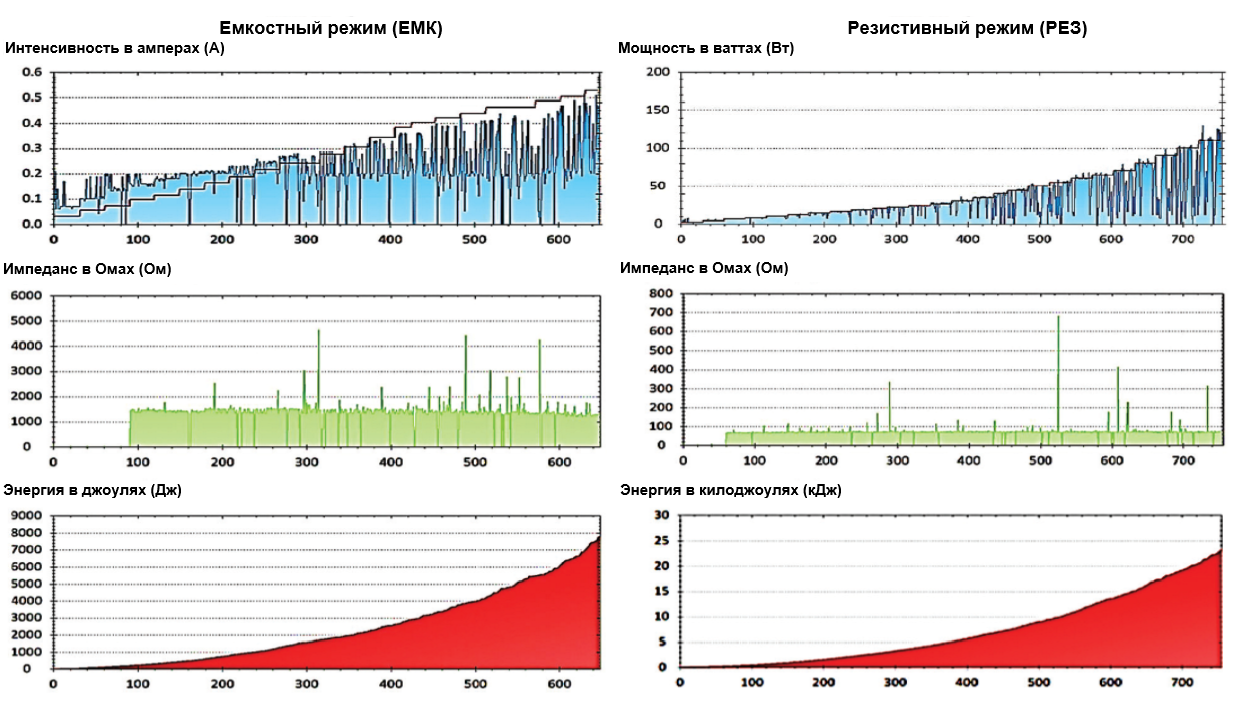
Рисунок 1. Графики выходных данных, полученные с помощью мониторинговой программы устройств. Отображаемые данные относятся к одному участнику (№ 8). По оси X отражены единицы последовательности мониторинга (более 1/с), а по оси Y — регистрируемый показатель.

Рисунок 2. Экспериментальная установка с емкостно-резистивным монополярным радиочастотным устройством (CRMRF), работающим на частоте 448 кГц (Indiba), электродами и компьютерным ПО для мониторинга.
Экспериментальная часть
В день испытаний участников просили воздержаться от еды, напитков и интенсивных упражнений в течение 1 часа до начала эксперимента, чтобы во время сеансов их физиологическое состояние оставалось стабильным. Участники прошли анкетирование по опроснику пригодности к участию, отвечая на вопросы, которые в том числе касались всех недавно полученных травм или перенесенных заболеваний, а также признанных противопоказаний к радиочастотной терапии (беременность, наличие злокачественных новообразований, металлических или электронных имплантатов в организме). Затем проводилась оценка «термической чувствительности кожи» участников с использованием пробирок, наполненных водой с тремя различными температурами (± 0,5°C): 45°C (тепло), 35C (нейтрально) и 25°C (холодно). Для продолжения участия от участника требовалось отличить друг от друга три температурных уровня. После отсева у оставшихся участников производился сбор демографических и антропометрических данных.
Перед началом сеанса участников просили лечь на спину на медицинскую кушетку с переносом веса всего тела на валики (Рисунок 2). На нижней четверти передней поверхности правого бедра лентой выделался квадратный участок. Температуру кожи регистрировали в центре квадратного участка на ноге, подвергающейся воздействию, и на соответствующем участке ноги, которая воздействию не подвергалась. Нога, не проходящая терапию, служила контрольным эталоном. Одновременно проводился контроль внутренней температуры тела (барабанной перепонки уха). Измерения температуры на участке кожи повторяли каждые 2 мин до полной стабилизации. Затем стабилизированную температуру брали за температуру кожи в ее исходном состоянии. На нейтральный пластинчатый электрод наносили слой токопроводящего крема толщиной 20 мл, и электрод помещали под брюшко икроножной мышцы на четверть расстояния от головки малоберцовой кости до латеральной лодыжки на ноге, подвергаемой воздействию.
Воздействие током емкостно-резистивной монополярной РЧ проводили активным электродом через слой крема толщиной 20 мл на отмеченном лентой квадратном участке. Интенсивность воздействия начиналась с самого низкого уровня, предусмотренного устройством, и через каждые 30 с повышалась на один уровень вверх. В такт движению метронома активным электродом на коже рисовались четкие круги со скоростью «один в секунду». Участники получили инструкции четко и оперативно сообщать о трех контрольных моментах: Первый – когда они начинают ощущать тепло на коже (начало теплового ощущения), второй – когда они ощущают умеренное, но комфортное тепло (четко выраженное тепловое ощущение), и третий – когда тепло начинает причинять дискомфорт (начало теплового дискомфорта). При этом регистрировалось время всех трех контрольных моментов и соответствующая интенсивность воздействия. Терапия прекращалась, как только достигалась точка «начала теплового дискомфорта».
После очистки участка воздействия после терапии проводилась регистрация (пиковой) температуры кожи на каждой ноге в том же самом месте, которое было использовано для измерения температуры в исходном состоянии. В это же самое время снимались показания внутренней температуры тела. Измерение температуры кожи повторяли (во время посттерапевтического наблюдения) последовательно каждые 30 с на ноге, прошедшей терапию, и каждые 5 минут на контрольной ноге в течение следующих 45 минут или до тех пор, пока температура на участке воздействия не возвращалась к исходному уровню (в зависимости от того, что наступало раньше).
В конце эксперимента также проводились повторные измерения внутренней температуры тела, комнатной температуры и влажности. Кроме того, отдельно в течение короткого времени проводился второй эксперимент, направленный на картирование изменений температуры активных электродов, использованных для РЧ-воздействия, на различных этапах исследования в ответ на задаваемую интенсивность энергии емкостно-резистивной монополярной РЧ (выраженную в процентах). С этой целью выбирались три произвольных уровня интенсивности наряду с четвертым уровнем, представляющим собой усредненную пиковую мощность, достигаемую в каждом режиме во время главного эксперимента.
Анализ данных
Все данные прошли обработку и анализ с использованием Microsoft Office Excel (версия 2010, Microsoft Corporation) и IBM SPSS Statistics (версия 20) для Windows. Групповые данные сравнивались с использованием модели двустороннего дисперсионного анализа с повторными измерениями (ANOVA) с апостериорным сравнением по методу Бонферрони по показателям теплового ответа в емкостном и резистивном режимах в трех временных точках (исходное состояние, состояние сразу после терапии и состояние через 45 минут после терапии в период наблюдения). Статистическая значимость выставлялась на уровне p ≤ 0,05 (0,8 P, 95% ДИ).
 Таблица 1. Демографические и усредненные (± СО)
антропометрические
данные 15 участников, прошедших локальное воздействие током емкостно-резистивной монополярной
радиочастоты
(CMRRF) равной 448 кГц.
Таблица 1. Демографические и усредненные (± СО)
антропометрические
данные 15 участников, прошедших локальное воздействие током емкостно-резистивной монополярной
радиочастоты
(CMRRF) равной 448 кГц.
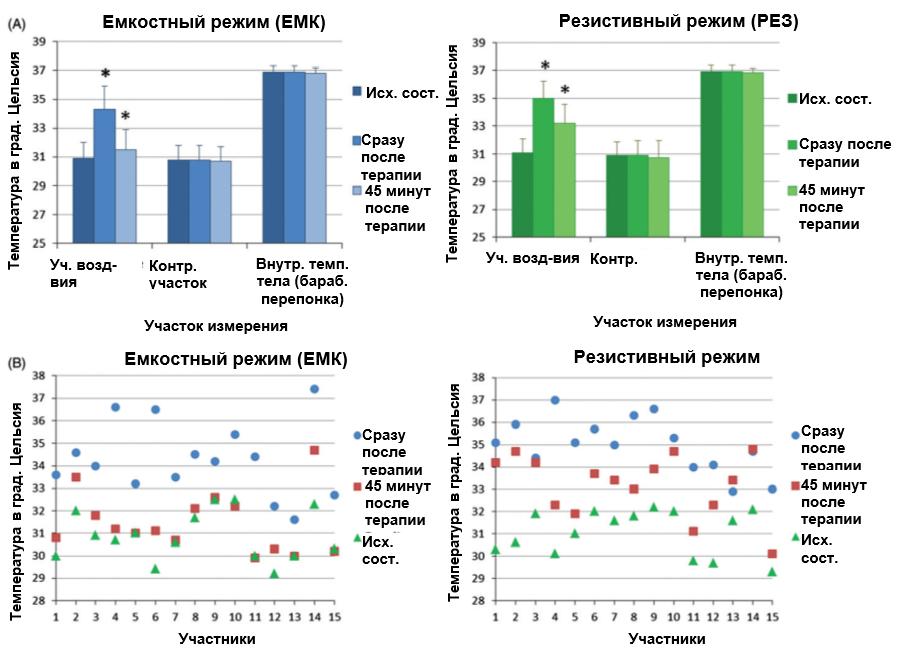 Рисунок 3. (A) Средние значения термических ответов кожи
на
локализованное воздействие током емкостно-резистивной монополярной радиочастоты (CRMRF) равной
448 кГц в
емкостном (ЕМК) и резистивном (РЕЗ) режимах. Отображаемые данные (исходное состояние, сразу
после терапии и
в течение 45 минут после терапии) получены по 15 участникам. *Статистически значимые отличия от
исходного
состояния (при p<0,05) (двусторонний дисперсионный анализ с повторными измерениями). (B)
Индивидуальные
значения термических ответов кожи на локализованное воздействие током емкостно-резистивной
монополярной
радиочастоты (CRMRF) равной 448 кГц в емкостном (ЕМК) и резистивном (РЕЗ) режимах (только
участок
воздействия). Отображаемые данные (исходное состояние, сразу после терапии и в течение 45 минут
после
терапии) получены по 15 участникам.
Рисунок 3. (A) Средние значения термических ответов кожи
на
локализованное воздействие током емкостно-резистивной монополярной радиочастоты (CRMRF) равной
448 кГц в
емкостном (ЕМК) и резистивном (РЕЗ) режимах. Отображаемые данные (исходное состояние, сразу
после терапии и
в течение 45 минут после терапии) получены по 15 участникам. *Статистически значимые отличия от
исходного
состояния (при p<0,05) (двусторонний дисперсионный анализ с повторными измерениями). (B)
Индивидуальные
значения термических ответов кожи на локализованное воздействие током емкостно-резистивной
монополярной
радиочастоты (CRMRF) равной 448 кГц в емкостном (ЕМК) и резистивном (РЕЗ) режимах (только
участок
воздействия). Отображаемые данные (исходное состояние, сразу после терапии и в течение 45 минут
после
терапии) получены по 15 участникам.
Результаты
Как и ожидалось, все 15 участников завершили оба сеанса исследования и прошли этап оценки. Радиочастотная терапия хорошо переносилась. Отсутствовали сообщения о каких-либо побочных эффектах, являющихся следствием вмешательства, включая проблемы, связанные с возможным перегревом. Демографические и усредненные (± СО) антропометрические данные участников представлены в Таблице 1.
Средние значения (± СО) теплового ответа кожи, а также индивидуальные образцы тепловых ответов, полученные от всех 15 участников после воздействия током емкостно-резистивной монополярной радиочастоты в емкостном и резистивном режимах, представлены на Рисунках 3(A-B), 4(A-B) и 5(A-B). Средние значения (± СО) температуры кожи в исходном состоянии, сразу после терапии и в течение 45 минут после терапии в емкостном режиме составили соответственно 30,9 (± 1,1)°C, 34,3 (± 1,6)°C и 31,5 (± 1,4)°C , а в резистивном режиме соответственно – 31,1 (± 1,0)°С, 35,0 (± 1,2)°С и 33,2 (± 1,4)°С. В Таблице 2 показаны средние значения (± СО) фактического времени, переданной энергии и пиковой выходной мощности, необходимые для достижения каждой тепловой стадии. На Рисунке 6(A-C) показаны индивидуальные данные среднего времени, средней энергии и средней пиковой мощности по участникам, указанные в Таблице 2 .
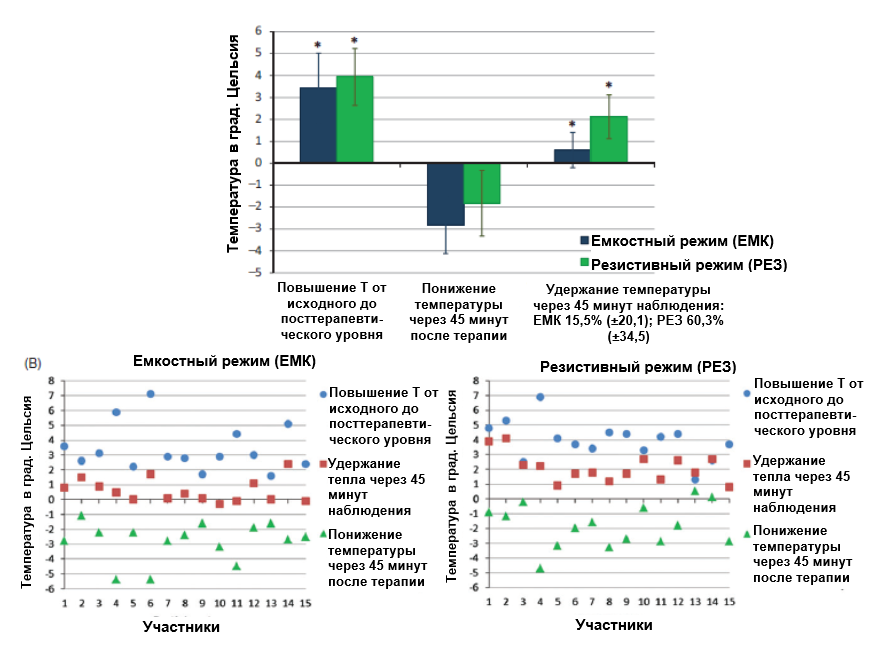
Рисунок 4. (A) Средние значения изменений температуры кожи в ответ на локализованное воздействие током емкостно-резистивной монополярной радиочастоты (CRMRF) равной 448 кГц в емкостном (ЕМК) и резистивном (РЕЗ) режимах. Отображаемые данные (повышение температуры, понижение температуры и удержание кожей температуры) представляют собой изменения от исходного состояния у 15 участников. *Статистически значимые отличия от исходного состояния (при p<0,05) (двусторонний дисперсионный анализ с повторными измерениями). (B) Индивидуальные значения изменений температуры кожи в ответ на локализованное воздействие током емкостно-резистивной монополярной радиочастоты (CRMRF) равной 448 кГц в емкостном (ЕМК) и резистивном (РЕЗ) режимах. Отображаемые данные (повышение температуры, понижение температуры и удержание кожей температуры) представляют собой изменения от исходного состояния у 15 участников.
Существенной разницы между исходной температурой кожи в двух группах не наблюдалось. В целом, наблюдалась статистически значимая разница между характерами теплового ответа в емкостном и резистивном режимах (F (1, 14) = 16,639, p = 0,001), хотя максимальные значения температуры кожи на момент окончания терапии существенно не отличались. Наблюдаемое увеличение средней температуры кожи от исходного до максимума составило 11,1% в емкостном и 12,7% в резистивном режиме.
В обоих режимах, емкостном и резистивном, также наблюдалось хорошее удержание набранной температуры через 45 минут после терапии по сравнению с исходным состоянием (ЕМК: F (1, 14) = 8,690, р = 0,011; РЕЗ: F (1, 14) = 70,321, р<0,001). Однако процентная доля удержания температуры через 45 мин терапии в резистивном режиме была значительно выше, чем в емкостном режиме (соответственно 53,6% и 17,5%) (F (1, 14) = 36,173, p< 0,001).
Апостериорный анализ мощности с использованием ПО G*Power (версия 3.1) подтвердил фактическую мощность результатов, полученных дисперсионным анализом ANOVA, равную 1,0. Во всех группах значимых изменений в термическом ответе контрольного участка кожи, не подвергнутого воздействию, равно как и изменений внутренней температуры тела (барабанной перепонки) ни на каком этапе отмечено не было. Изменения температуры, зарегистрированные на двух активных электродах во время второго эксперимента, представлены в Таблице 3 .
Разбор результатов
На настоящий момент имеются обширные научные исследования, посвященные изучению термофизиологических эффектов воздействия токов РЧ на биологические системы. Большинство опубликованных исследований в этой области было проведено на лабораторных животных, с особым упором на грызунов. Существует устойчивое мнение, что эти мелкие млекопитающие представляют собой слабое подобие модели человека, поскольку их физиологические механизмы потери тепла ограничены, что затрудняет экстраполяцию результатов исследований на человека [6]. Так, грызуны (особенно мыши) обладают более высокой термонейтральной зоной - на уровне примерно 30 °C, тогда как у людей (в одежде) она находится на уровне 22-25 °C [19-21]. В настоящем эксперименте средняя (± СО) комнатная температура составляла 24,0 (± 0,8)°C в емкостном и 23,9 (± 1,2)°C в резистивном режиме. Оба значения попадают в диапазон термонейтральной зоны человека.
Вызов теплового ответа воздействием энергией в радиочастотном диапазоне на тело человека зависит от многих волновых параметров, таких как частота, интенсивность, продолжительность воздействия и площадь участка тела, на которую оказывается воздействие. Прогнозирование теплового ответа в клинических условиях на основе только существующих моделей является сложной задачей. Проведенная экспериментальная и теоретическая работа указывает на то, что при низких уровнях интенсивности «демодуляция» радиочастот целесообразна только на частотах намного ниже нескольких МГц. Другими словами, биологические системы не обладают возможностью эффективно «выпрямлять» РЧ-поля выше нескольких МГц так, чтобы они могли воздействовать на эндогенные поля организма и биологические процессы [13].
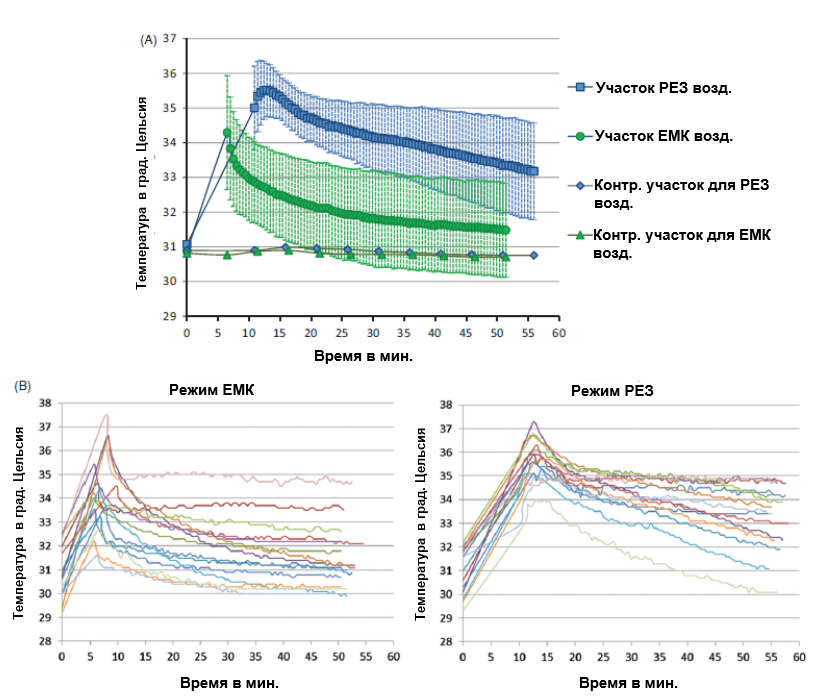
Рисунок 5. (A) Средние значения падения температуры кожи после локализованного воздействия током емкостно-резистивной монополярной радиочастоты (CRMRF) равной 448 кГц в емкостном (ЕМК) и резистивном (РЕЗ) режимах. Данные получены по 15 участникам и отражают процесс остывания участка кожи в течение 45 минут наблюдения после РЧ-воздействия. (B) Индивидуальные значения падения температуры кожи после локализованного воздействия током емкостно-резистивной монополярной радиочастоты (CRMRF) равной 448 кГц в емкостном (ЕМК) и резистивном (РЕЗ) режимах. Данные получены по 15 участникам и отражают процесс остывания участка кожи в течение 45 минут наблюдения после РЧ-воздействия.
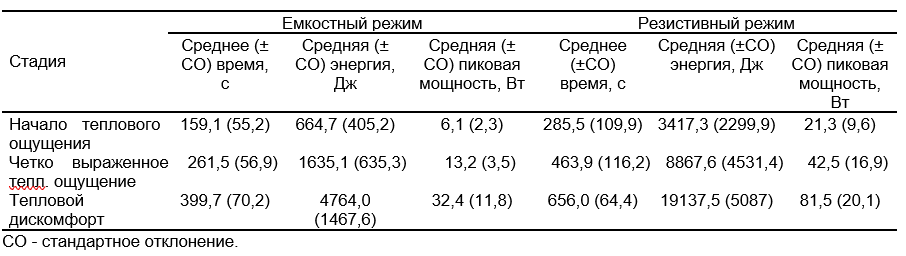
Таблица 2. Среднее время, средняя энергия и средняя пиковая мощность, достигнутые на каждой из трех стадий теплового ответа у 15 участников, прошедших емкостно-резистивную монополярную радиочастотную терапию (CRMRF) с частотой 448 кГц на участке кожи.
Радиочастотные волны могут взаимодействовать с биологическими тканями посредством ряда механизмов. При общей хорошей изученности теории, лежащей в основе теплового эффекта радиочастотного взаимодействия, научные утверждения о «так называемых» нетепловых эффектах воздействия на низком РЧ-уровне (LLNT) несколько противоречивы и не подтверждаются в достаточной мере экспериментальными данными [13]. Хотя механизмы нетеплового взаимодействия могут напрямую не быть связанными с повышением температуры в тканях, даже на очень низких уровнях радиочастот тепловые эффекты все же имеют место, поскольку все взаимодействия между радиочастотными полями и биологическими тканями приводят к передаче тканям энергии, что в конечном итоге вызывает повышение температуры [22]. Так, на клеточный метаболизм могут влиять изменения температуры даже в доли градуса [13]. Однако, как было установлено, большая часть эффектов от нагрева на физиологическом уровне проявляется при повышении температуры не менее чем на 2°C.
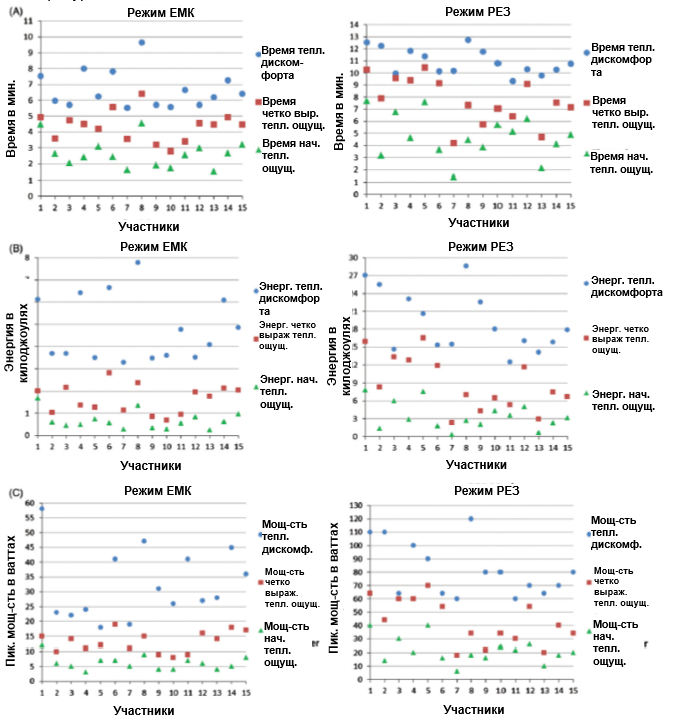
Рисунок 6. (A) Индивидуальные значения термических ответов кожи на локализованное воздействие током емкостно-резистивной монополярной радиочастоты (CRMRF) равной 448 кГц в емкостном (ЕМК) и резистивном (РЕЗ) режимах (только участок воздействия) в конкретный момент времени. Отображаемые данные (начало теплового ощущения, четко выраженное тепловое ощущение и температурный дискомфорт) получены по 15 участникам. (B) Индивидуальные значения термических ответов кожи на локализованное воздействие током емкостно-резистивной монополярной радиочастоты (CRMRF) равной 448 кГц в емкостном (ЕМК) и резистивном (РЕЗ) режимах (только участок воздействия) для конкретных значений энергии. Отображаемые данные (начало теплового ощущения, четко выраженное тепловое ощущение и температурный дискомфорт) получены по 15 участникам. (C) Индивидуальные значения термических ответов кожи на локализованное воздействие током емкостно-резистивной монополярной радиочастоты (CRMRF) равной 448 кГц в емкостном (ЕМК) и резистивном (РЕЗ) режимах (только участок воздействия) для конкретных значений (пиковой) мощности. Отображаемые данные (начало теплового ощущения, четко выраженное тепловое ощущение и температурный дискомфорт) получены по 15 участникам.
Степень проявления эффекта, вызываемого процедурами нагрева (средствами электрофизического воздействия), на физиологическом уровне зависит от типа энергии, передаваемой устройством, и от глубины проникновения энергии [23]. Так, считается, что воздействие током импульсной РЧ с большей вероятностью способно вызвать определенные биологические ответы, чем воздействие током непрерывной РЧ при той же средней плотности падающего импульса. Точно так же, если низкопроникающая ИК-энергия (не РЧ-диапазона) поглощается в самых поверхностных слоях кожи, что приводит к поверхностному нагреву, поглощение радиочастот будет иметь сложный комплексный характер и будет проходить на другой глубине [6], что может потенциально вызвать более глубокий нагрев и, следовательно, более глубокое воздействие. Хотя данное исследование и не ставило перед собой задачу измерения параметров глубинного нагрева, по сообщениям ряда других исследователей, глубинный нагрев может достигаться средствами электрофизиологического РЧ-воздействия, более эффективно вызывая при этом определенные физиологические эффекты, например, более эффективно увеличивая растяжимость тканей по сравнению с поверхностным нагревом [24,25].
Результаты настоящего исследования показывают существенные различия между характерами нагрева тканей в емкостном и резистивном режимах радиочастотной монополярной терапии по показаниям кожного термометра. В емкостном режиме ответы на всех трех тепловых стадиях (начало ощущения, четко выраженное ощущение и дискомфорт) достигались значительно быстрее, однако при этом набранная температура падала быстрее и удерживалась в меньшей степени, чем в резистивном режиме. При этом, в связи с отсутствием линейной зависимости между настройками интенсивности в двух режимах дальнейшее их сравнение становится проблематичным. Аналогичным образом отсутствие линейной зависимости затронуло бы и пиковую мощность, достигнутую на каждом временном этапе. Полученные индивидуальные данные (Рисунок 4B) говорят о том, что в любом режиме чем больше повышение температуры, вызванное нагревом, тем больше будет падение температуры на последующем этапе.
Как указывается, средняя (± СО) пиковая температура кожи составила 34,3 (± 1,6)°C в емкостном режиме и 35,0 (± 1,2)°C в резистивном режиме (Рисунок 3A). Самая высокая температура, зарегистрированная у кого-либо из конкретных участников, составила 37,4°C в емкостном и 37,0°C в резистивном режиме (Рисунок 3B). Сами по себе эти значения ниже или едва достигают внутренней температуры тела. Это означает, что в лучшем случае удается достичь только «легкой гипертермия» и исключительно по отношению к исходной температуре кожи, зарегистрированной на участке воздействия. Чтобы называться гипертермией, температура должна быть повышена до супрафизиологического уровня, то есть примерно до 40-45°C или даже выше в случае термической абляции. Как показали лабораторные исследования клеток, цитотоксические эффекты тепла и гибель клеток проявляются в диапазоне температур 40–55°C, при этом «точка перелома» наблюдается при температуре примерно 43°C [26-29].
Для количественной оценки термических доз, полученных во время термического воздействия, часто применяется суммарная или эквивалентная термическая доза [30]. Суммарная или общая эквивалентная термическая доза может выражаться в виде количества кумулятивных эквивалентных минут (CEM) по отношению к произвольно выбранной температуре 43°C (CEM 43), как первоначально было предложено учеными Сапарето и Дьюи [31]. С помощью этого метода любую функциональную зависимость «время-температура» можно преобразовать в одно число - «дозу термического изоэффекта», которое представляет собой эквивалентное количество минут нагревания при температуре 43°C. Для соответствующего расчета используется следующая формула при условии, что температура остается постоянной:

где СЕМ 43°С — суммарное число эквивалентных минут при температуре 43°С, t — время (длительность) воздействия, R — константа, связанная с температурной зависимостью коэффициента гибели клеток (R (Т<43 °С ) = 0,25, R (T>43 °C) = 0,5) и T — температура в течение времени t.
В случае сложной функциональной зависимости «температура-время» CEM 43°C вычисляется по каждому мелкому интервалу времени (t), во время которого температура (T) остается относительно постоянной, а потом полученные результаты суммируются за весь период по формуле:
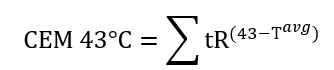
где Tavg — средняя температура на каждом временном интервале (t). Полученное значение CEM 43°C представляет собой эффект всей длительности теплового воздействия. Оценочные значения «дозы термического изоэффекта» используются преимущественно в дозиметрии термотерапии рака и в аппаратах магнитно-резонансной томографии (МРТ) [30]. Вычисление оценочных значений может выполняться также и для емкостно-резистивной монополярной РЧ-терапии, учитывая имеющиеся данные проведенных исследований по вызову гипертермии для лечения рака[18,32-34] и других клеточных эффектов [17] с использованием РЧ-терапии.
В настоящем исследовании во время РЧ-воздействия измерялись только исходная и пиковая температуры. Если предположить, что достигнутая пиковая температура поддерживалась на протяжении всей длительности терапии у каждого участника, то можно рассчитать среднюю (± СО) термическую дозу СЕМ 43 °C для выборки, которая составляет 0,0004 (± 0,0008) мин в емкостном и 0,0005 (± 0,0008) мин в резистивном режиме. Однако этот расчет применим только к тому участку кожи, на котором производились измерения температуры. Подобную оценку для более глубинных тканей, где термическая доза могла бы быть совершенно другой, по текущим данным дать невозможно.
Пиковые мощности, представленные в Таблице 2 и на Рисунке 6 (C), не всегда точно отражают мощность тока при емкостно-резистивной монополярной РЧ-терапии (CRMRF), необходимую для достижения трех временных точек при проведении обычного сеанса терапии, когда установленная терапевтическая доза может подаваться с самого начала. Они скорее обозначают пиковые мощности, которые могут быть достигнуты, если увеличивать интенсивность постепенно каждые 30 секунд, начиная с минимальной дозы. Среднее значение (± СО) средней мощности (СМ) («общая средняя мощность» воздействия на каждого участника в течение всего срока терапии), подаваемой для достижения стадий начала теплового ощущения, четко выраженного теплового ощущения и и температурного дискомфорта, составило соответственно 3,89 (± 0,99), 6,05 (± 1,36) и 11,70 (± 1,67) Вт в емкостном и 10,61 (± 3,78), 17,87 (± 5,36) и 28,74 (± 4,74) Вт в резистивном режиме.
Температура кожи на стадиях «начало теплового ощущения» и «ярко выраженное тепловое ощущение» не регистрировалась, так как это бы нарушило непрерывность терапии и задержало бы наступление последующей термической стадии в связи с «термическим вымыванием». Достигнутые в двух режимах пиковые температуры кожи существенно друг от друга не отличались, несмотря на нелинейность соответствующих настроек интенсивности. Тем не менее, если в емкостном режиме наблюдалось резкое снижение (средней) температуры кожи сразу после терапии, то в резистивном режиме в первые несколько минут после окончания терапии напротив наблюдалось повышение температуры. Маловероятно, что на столь разный характер тепловыделения могли повлиять настройки интенсивности.
В резистивном режиме удалось удержать более 60 % полученного тепла (в среднем (± СО) - 60,3 (± 34,5)%) на момент окончания 45-минутного периода наблюдения, ср. с 15 % (в среднем (± СО) - 15,5 (± 20,1)%) в емкостном режиме (Рисунок 4A). Температура контрольного участка, не подвергавшегося воздействию, и внутренняя температура тела не претерпели существенных изменений ни при одном из условий. Если тот факт, что внутренняя температура не изменилась, удивления не вызывает, поскольку местное воздействие радиочастотной энергии на внутреннюю температуру влиять не должно [6], результаты по контрольному участку все же противоречат эффекту «перекрестного действия» (нежелательный эффект, возникающий на соседнем участке, не подвергающемся воздействию), о котором сообщалось при применении коротковолновой терапии (SWT) [35]. Это может быть связано с потенциально более низким уровнем «рассеяния» волн при проведении емкостно-резистивной монополярной РЧ-терапии по сравнению с коротковолновым воздействием.

Таблица 3. Температура электрода (активного) на разных временных этапах и интенсивность воздействия во время проведения локализованной емкостно-резистивной монополярной РЧ-терапии (CRMRF) на частоте 448 кГц. Исследование проводилось с одним участником мужского пола в возрасте 37 лет (индекс массы тела - 23) при комнатной температуре 25°С и влажности 66%.
Более быстрый нагрев и более быстрое снижение температуры в емкостном режиме могут свидетельствовать об относительно поверхностном характере проникновения. По аналогии с «емкостным методом» воздействия коротковолновой терапии емкостной (фарадический) эффект в тканях может вызываться более высокой долей «электрического» (E), чем «магнитного» (H) поля [4,11]. Соответственно поверхностными тканями (кожей и жировыми слоями) поглощается больше энергии, чем более глубинными тканями (подлежащими тканями, такими как мышцы), поскольку концентрация поля в поверхностных тканях выше [36,37].
Точно так же резистивный режим РЧ-терапии сравним с «индуктивным методом» коротковолновой терапии, поскольку оба создают эффект, вызванный по большей части магнитным (H) полем [4,11]. Более высокий показатель удержания тепла и факт отсутствия резкого падения температуры после терапии убедительно свидетельствуют о более высоком проникновении энергии. Если при индукционной терапии поглощение энергии выше в более глубинных тканях, таких как кровь и мышцы, из-за их более низкого сопротивления и более высокого содержания электролитов, то такие ткани, как кожа и подкожный жир, которые имеют более высокое сопротивление, поглощают меньше энергии и, следовательно, меньше нагреваются по сравнению с более глубинными тканями [11,37].
Количество выделяемого тепла пропорционально проводимости тканей и напряженности поля [4]. На проникновение радиочастотной энергии также влияет размер используемых в терапии электродов – более крупные обладают большей проникающей способностью, чем электроды меньшего размера [11]. Между коротковолновой терапией и емкостно-резистивной монополярной РЧ-терапией есть принципиальное различие, если учитывать частоту и другие характеристики применяемых ими РЧ-волн. По этой причине все физические принципы взаимодействия между короткими волнами и тканями скорее всего не применимы к емкостно-резистивной монополярной РЧ-терапии. По сравнению с КВ-терапией исследований физических принципов взаимодействия емкостно-резистивных монополярных РЧ-волн с тканью было опубликовано мало.
На результаты, полученные в данном исследовании, вероятнее всего повлияли размер (крупный; диаметр 65 мм) и геометрическая форма (круглая) применяемых активных электродов, количество оставляемого на коже токопроводящего крема и другие индивидуальные факторы, такие как анатомия участка воздействия, сопротивление тканей и, возможно, антропометрические факторы (например, процент жира в организме, индекс массы тела).
Следует отметить, что влияние подобных индивидуальных факторов на анализ полученных результатов можно было бы свести к минимуму за счет перекрёстного планирования исследования.
Размер используемого электрода соответствовал размеру участка воздействия, что потенциально способствовало однородному распределению поля. Размер электрода влияет на величину генерируемого электромагнитного поля и плотность поля/ тока [11]. При использовании крупных электродов плотность поля под активным электродом не была бы непропорционально высокой, что способствовало бы более равномерному распределению энергии. Изучение плотности поля/ тока представляет собой отдельное направление, которое выходит за рамки анализа настоящей работы.
Как показано в Таблице 3 , температура активных электродов при той же интенсивности емкостно-резистивного монополярного РЧ-воздействия, что и в главном эксперименте, существенно не отличались от достигнутой пиковой температуры кожи. Пиковая температура электрода в резистивном режиме оставалась постоянно ниже, чем температура кожи, в то время как в емкостном режиме температура электрода незначительно увеличивалась, когда интенсивность воздействия поддерживалась в течение более длительного срока, что говорит о том, что повышение температуры кожи не было прямым результатом контактного нагревания горячим электродом, а скорее результатом взаимодействия РЧ с тканью.
Участники в большинстве случаев сообщали о более поверхностном «ощущении» нагревания в емкостном режиме, при этом нагревание ими ощущалось главным образом на коже внутри участка воздействия. Были сообщения о слабом ощущении тепла через коленный сустав или в икроножной мышце. При этом по сообщениям участников «ощущение» в резистивном режиме было более глубоким и однородным и также отдавалось в коленный сустава и голень.
Не следует забывать, что все утверждения о восприятии тепла глубинными тканями организма следует толковать с осторожностью, поскольку локализованное тепловое восприятие основано в первую очередь на ощущениях кожных рецепторов [2], и до сих пор есть некоторые разногласия относительно того, является ли тепловое восприятие глубинными тканями тепловым восприятием в чистом виде или его следует трактовать как ноцицепцию. На сегодняшний день научных доказательств существования субъективного восприятия температуры более глубинными тканями, такими как мышцы, недостаточно [38]. Есть вероятность существования механизма теплового восприятия на глубине, но он может существовать и только на подсознательном уровне, когда температура тканей находится в пределах примерно 25-41°С. Восприятие мышцами температуры, выходящей за пределы этого диапазона, по мнению некоторых ученых является менее сильным по сравнению с ноцицепцией. Кроме того, все еще под вопросом, могут ли ноцицепторы и другие прессорные и механочувствительные рецепторы в мышцах функционировать как периферийные органы чувств, вызывая у людей субъективные температурные ощущения [38,39].
Ощущение тепла в тканях зависит от характера передачи тепловой энергии (например, от изменения температурных условий, скорости изменения температуры) [1,2,6]. В связи с этим предполагается, что, хотя глубинный нагрев и мог иметь место в результате емкостно-резистивной монополярной РЧ-терапии, те различные ощущения нагрева, о которых сообщали участники исследования в емкостном и резистивном режимах, могут быть связаны с разницей в скорости и распределении температурных изменений в более поверхностных тканях, таких как кожа и подкожная фасция, где имеются терморецепторы.
Любую возможную вариабельность данных термического ответа тканей, наблюдаемую в настоящем исследовании между отдельными участниками, можно объяснить вариабельностью их антропометрических факторов. Хотя это и не входило в основные задачи исследования, была проанализирована корреляция между антропометрическими факторами и тепловыми ответами участников, что позволило оценить возможность прогнозирования тепловых ответов человека на основе его антропометрических и исходных данных, используя статистическую модель (линейной регрессии).
Процентное содержание жира в организме характеризовалось умеренной отрицательной корреляцией (с уровнем значимости p<0,05) при исследовании данных начала теплового ощущения и теплового дискомфорта в емкостном режиме, в то же время в резистивном режиме аналогичные показатели наблюдались только по тепловому дискомфорту. Кроме того, в резистивном режиме умеренная отрицательная корреляция (с уровнем значимости р<0,05) наблюдалась между комнатной температурой и данными начала тепловых ощущений и данными четко выраженных тепловых ощущений. Никаких других корреляций антропометрических факторов с данными теплового ответа обнаружено не было. Таким образом можно сделать вывод, что на основе данных настоящего исследования невозможно определить соответствующую статистическую модель прогнозирования теплового ответа и терапевтические дозы воздействия ни в одном из режимов.
Насколько известно авторам, настоящее исследование является первым в своем роде исследованием, изучающим тепловые ответы кожи на локальное терапевтическое воздействие тока в радиочастотном диапазоне ниже КВ-диапазона. Был обнаружен целый ряд исследований тепловых ответов кожных и (или) глубинных тканей человека на воздействие в РЧ-диапазоне (преимущественно в коротковолновом) [35,40-47], но только в незначительном количестве таких исследований проводилось картирование температуры кожи в течение столь долгого периода посттерапевтического наблюдения, как 45 минут. Во многих исследованиях, опубликованных ранее, сообщалось о значительном повышении и хорошем удержании температуры как на кожных покровах, так и внутри мышечных тканей [40,42,43,47].
Из самых последних (неинвазивных) исследований, в которых изучались нарастающие дозы воздействия импульсной КВ-терапии, стоит упомянуть исследование Брикнелла и Уотсона [41], в котором сообщалось о параметрах дозы, приводящих к «возможному тепловому восприятию» (среднее «средней мощности (СМ)» 6,58 (± 3,50) Вт) и «четко выраженному тепловому восприятию» (среднее СМ 10,88 (± 3,32) Вт) на коже. В исследовании сообщалось о повышении средней температуры на 2,10°C от исходного уровня до стадии «четко выраженного теплового восприятия». В другом исследовании, Аль-Мандил и Уотсон [35] сообщают о значительном повышении температуры кожи при высоких (ср. мощность 24 Вт) и низких (ср. мощность 3 Вт) дозах воздействия при проведении импульсной КВ-терапии.
Среди исследований инвазивного воздействия следует сказать о работах Дрейпера и др. [44], которые исследовали изменения температуры внутри икроножной мышцы в ответ на 20-минутное воздействие импульсной КВ-терапии (ср. мощность 48 Вт). После процедуры было зарегистрировано среднее (± СО) повышение температуры на 3,49 (± 1,13)°C, а в первые 10 минут после терапии было зарегистрировано снижение температуры на 1,78 (± 0,69)°C. Позже, в своем исследовании некоротковолнового воздействия Такахаши и др. [45] сообщали о повышении температуры внутри коленного сустава на 5°C при 20-минутной импульсной РЧ-терапии (8 МГц, 200 Вт) у пациентов, страдающих остеоартритом колена. Падение температуры в этом исследовании не отслеживалось.
К потенциальным ограничениям настоящего исследования следует отнести невозможность отслеживания изменений температуры в глубинных тканях, несмотря на то, что по результатам было видно, что в более глубинных тканях могло происходить значительное поглощение тепла. В то время как подходящие неинвазивные методы измерения температуры в глубинных тканях авторам были недоступны, с инвазивными методами измерения температуры существует ряд потенциальных проблем. Так, в тех случаях, когда устройство регистрации температуры (термопары или термисторы) оставалось на месте регистрации во время воздействия током РЧ-диапазона (как в исследовании Такахаши и др. [45]), существовла большая вероятность того, что электромагнитное поле могло непосредственно нагреть измерительное устройство и тем самым вызвать более высокие температурные показания. Кроме того, инвазивная процедура вызывает в тканях воспалительную реакцию, которая может влиять на локальную физиологическую активность (например, на изменение кровотока на участке воздействия).
Неинвазивное измерение температуры в глубинных тканях с использованием таких методов, как магнитный резонанс (МР-термометрия) и ультразвук (УЗ-термометрия), получает все большее распространение и начинает активно применяться в таких областях, как термотерапия рака [48-51]. Подобные методы отличаются повышенной сложностью и выходят за рамки данного исследования. Тем не менее, в будущем следует приветствовать проведение подобных исследований с использованием комплексных неинвазивных систем измерения при изучении тепловых ответов более глубинных тканей на воздействие емкостно-резистивной монополярной РЧ-терапии.
Помимо температуры глубинных тканей в данном исследовании также не регистрировалась температура кожи на стадиях начала теплового ощущения и четко выраженного теплового ощущения. Принимая во внимание методологию, выбранную для проведения данного эксперименте, измерение и регистрация температуры без существенного влияния на непрерывность лечения в данном случае была бы затруднительна.
Аналогично, описанные здесь профили теплового ответа применимы только к размеру активных электродов (65 мм), используемых в данном эксперименте, по соображениям плотности электрического поля и к подвергнутому воздействию участку тела по анатомическим соображениям. Кроме того, на наступление термических стадий могли повлиять термические свойства токопроводящего крема и количество крема, оставшегося на участке воздействия к концу процедуры.
Еще одним ограничением, часто встречающимся в лабораторных исследованиях, является молодость и хорошее физическое здоровье участников, что ограничивает обобщаемость результатов. В данном исследовании, хотя участники и были физически здоровы и активны, для облегчения обобщаемости их возрастной диапазон (19-59 лет) был намеренно оставлен широким. В любом случае экстраполяция результатов на популяцию пациентов проблематична, поскольку их физиологические ответы будут отличаться из-за фоновой патологии.
Заключение
Исследование подтверждает возможность значительного повышения и успешного удерживания температуры кожи как в емкостном, так и в резистивном режимах монополярной РЧ-терапии . Для обоих режимов терапевтического воздействия были определены средние значения времени, энергии и мощности, необходимые для достижения стадий начала тепловых ощущений, четко выраженных тепловых ощущений и теплового дискомфорта при постепенном увеличении доз воздействия (как описано).
Данное исследование не ставило перед собой цель дать рекомендации по дозировке воздействия на основе восприятия тепла, и сами по себе результаты не могут быть экстраполированы на популяцию пациентов. Тем не менее, полученные результаты могут служить руководством для клиницистов при принятии ими клинических решений, когда бы они не решили обратиться к подобной терапии. Исследование также способствует получению полезных исходных данных для дальнейших исследований низкочастотных диапазонов радиочастотной терапии, которые до сих пор остаются в значительной степени неизученными. Таким образом, необходимы дальнейшие исследования, направленные на устранение описанных ограничений и изучение других физиологических ответов (таких как кровоток, температура в глубинных тканях), а также клинические исследования с участием групп пациентов.
Благодарности
Авторы хотели бы поблагодарить всех сотрудников и студентов Университета Хартфордшира, которые любезно вызвались принять участие в этом исследовании и провели несколько часов своего драгоценного времени в лаборатории.
Декларация интересов
Университет Хартфордшира получает отраслевое финансирование исследований, связанных с этой научно-исследовательской программой (Indiba SA). Отраслевые спонсоры не участвовали в планировании исследования, сборе данных, анализе данных и подготовке текста. Ответственность за содержание и составление данной статьи несут только ее авторы.

